Las infecciones causadas por Helicobacter Pylori suponen un problema de salud a nivel mundial al estar involucradas en procesos carcinogénicos graves. Entre ellos el linfoma de la mucosa estomacal, cáncer gástrico o adenocarcinoma esofágico. Actualmente, debido a la alta resistencia que presenta la bacteria, se han evaluado diferentes tratamientos para conseguir su erradicación. Por ello, he querido exponerlos, actualizados y respaldados por diversas investigaciones que acompañaré en el artículo.
Patogenia y diagnóstico de Helicobacter pylori
Es una bacteria cosmopolita, se adapta fácilmente al medio donde vive. Se caracteriza por ser un germen muy influenciado por el pH que lo rodea, sobreviviendo en medios moderada y fuertemente ácidos, dotándole de una capacidad única en el mundo bacteriano para habitar el estómago. Este órgano generalmente es inviable como diana de parásitos, pues el jugo gástrico neutraliza casi todos los microorganismos que pasan por él. Helicobacter pylori ha ido desarrollando varios mecanismos de defensa y adaptación que le han permitido proliferar en muchas partes del estómago, como las criptas profundas, el interior de las células epiteliales o el moco gástrico. Es una bacteria anaerobia, necesitando mínimas cantidades de oxígeno, esto explica porque no se la encuentra en el colon.
Una vez instalada, su modus operandi se basa en:
- Segregar ureasas, que transforman la urea en dióxido de carbono y amoníaco. Normalmente el ciclo de la urea comienza en los hepatocitos, pero algunas bacterias como Helicobacter disponen de estas enzimas. Los productos de degradación ayudan a regular el pH para que no se torne muy ácido.
- Libera colagenasas y peptidasas. Estas enzimas van a deteriorar y penetrar la mucosa del estómago, que están conformada de proteínas ricas en colágeno.
- Forma espacial. Su estructura en forma de hélice le permite adherirse en las células epiteliales y taladrar literalmente el epitelio.
- Es gramnegativa. Posee una doble membrana lipídica que la protege de la agresión de los antibióticos convencionales.
- Sintetiza exopolisacáridos. De esta manera es capaz de fabricar películas o biofilms alrededor de su membrana, constituyendo así, una barrera defensiva contra linfocitos, pH agresivo y antibióticos.
- Producción de adhesinas. Estas proteínas le permiten pegarse y adherirse a las células epiteliales, suelen buscar sitios de unión específicos que dificulte la llegada de los antibióticos.
- Mutación celular. Una vez adheridas a la célula sana, le provocan una mutación que con el tiempo promueve la replicación de esta célula mutada. La disgregación favorece la migración de células tumorales a otras partes del cuerpo incentivando la carcinogénesis.
- Facilita la inflamación. Algunas citocinas mediadoras de la inflamación juegan un papel crucial en los procesos de adhesión celular. De acuerdo al esquema perigenético de la bacteria, la interleucina 6 y el TNF alfa, entre otros, pueden estimular la migración de células mutadas.
- Betalactamasas. Enzimas que neutralizan la acción antimicrobiana de las penicilinas. Obedecen a una clasifiación bastante amplia, aunque los expertos las dividen en 4 grupos. Las penicinilasas están en el grupo A, desactivadas normalmente por el ácido clavulánico o el sulbactam. Si hay una sobreproducción de betalactamasas o estas son más específicas, la resistencia se incrementa.
El diagnóstico habitual para detectarla y actuar en consecuencia consiste en pruebas de aliento, análisis serológico, cultivo de heces o endoscopia, como último recurso.
La prueba de aliento, no disponible en todos los centros hospitalarios, es algo cara, sin embargo, determina en gran medida si existe una infección por Helicobacter. Esta prueba nos confirma la invasión en el momento, es decir, si ahora mismo el paciente la está sufriendo.
El cultivo de heces se realiza de manera secundaria para establecer la presencia del antígeno fecal, que ayuda a conocer si el tratamiento está funcionando o si la infección sigue activa.
La prueba serológica, es decir, de anticuerpos, mide los niveles de IgM e IgG. Se busca esclarecer la sensibilidad del paciente. Si las inmunoglobulinas salen altas puede ser que haya una parasitosis o que la persona haya sufrido hace tiempo una infección. Helicobacter pylori puede volver a infectar un huésped aunque se la haya erradicado anteriormente. El organismo seguirá reflejando niveles altos de estos anticuerpos. Es una prueba que no determina con exactitud la presencia de una infección activa, de ahí que se use para ver si los niveles son altos o exageradamente elevados, considerando el historial clínico del paciente, el médico se hará una idea.
La mejor manera de diagnosticar una infección sería mediante endoscopia. Es una prueba definitiva y determina en el 99% de los casos la presencia de Helicobacter pylori. Se recoge una muestra de tejido de la mucosa del estómago y se lleva al departamento de histología para analizarla.
Tratamientos clínicos de 1º, 2º y 3º línea
El gran inconveniente que existe con una infección de Helicobacter pylori es la alta probabilidad de úlcera gástrica en la persona afectada. Si las úlceras no se curan pueden volverse rebeldes y cursar en cáncer. Por ello, la comunidad médica-científica hace mucho hincapié en adoptar los protocolos de primera línea cuanto antes entre 7-14 días. Durante y después del tratamiento se debe chequear si la bacteria responde positivamente al tratamiento y si se ha erradicado por completo.
Entre las zonas más afectadas citamos África, Asia, Latinoamérica y el Caribe.
Según las investigaciones y resultados recogidos en la revista de gastroenterología de Scielo Perú, en la imagen de abajo se muestran esquematizados los tratamientos de primera línea utilizados en varias regiones de Sudamérica, donde la incidencia de enfermedad por Helicobacter es más alta que en Europa.
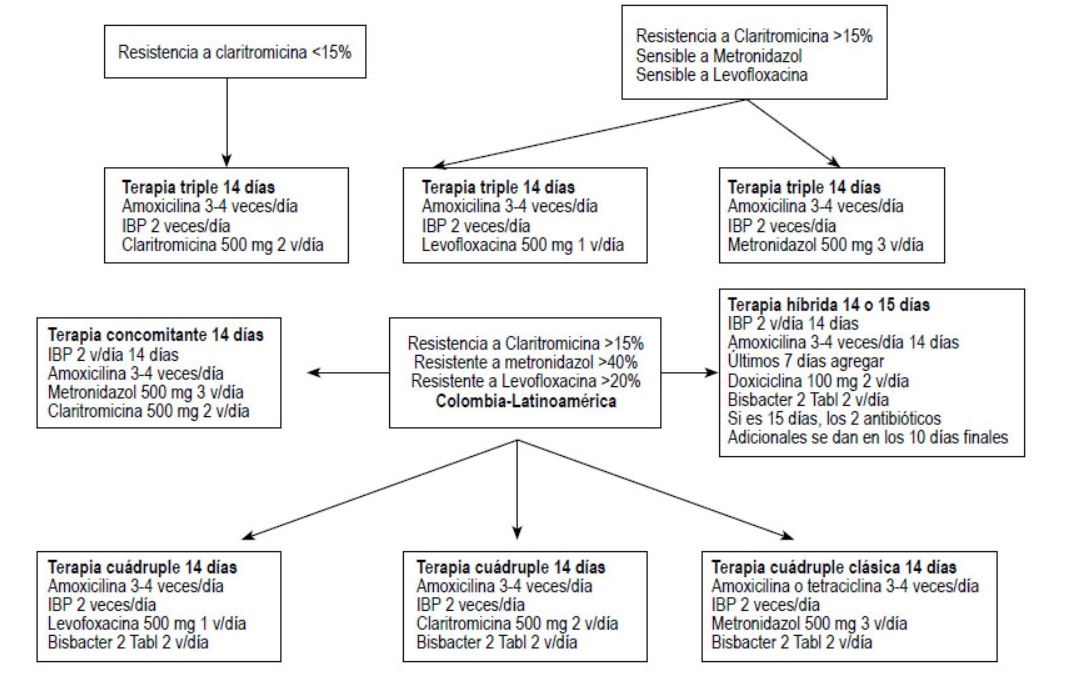
En España y otros países de Europa, se trabaja a nivel clínico con la triple y cuádruple terapia de primera y segunda línea. Este sistema es el siguiente:
- Inhibidor de la bomba de protones: Generalmente omeprazol, aunque también se utiliza ransoprazol y lansoprazol. El vonoprazan se ha comprobado que eleva todavía más los niveles de pH por su antagonismo con el potasio. Se utilizan los antiácidos para neutralizar el ácido y que la actividad antimicrobiana de los antibióticos sea mayor. Su efectivo preventivo contra úlceras es prioritario.
- Claritromicina. Helicobacter presenta una alta resistencia a este medicamento. La claritromicina se emplea para impedir la síntesis de ácidos ribonucleicos en la bacteria uniéndose al ribosoma 50S, pero como la bacteria tiene doble membrana y forma biopelículas, no consigue romper las defensas.
- Amoxicilina clavulánico. La amoxicilina inhibe la síntesis de la pared bacteriana, lo que anula su barrera de defensa principal, de esta manera las tetraciclinas o los macrólidos pueden ejercer actividad en su metabolismo. Se acompaña con ácido clavulánico para inactivar las betalactamasas y dejar a la bacteria vulnerable.
- Metronidazol. Es un antiparasitario que se emplea en terapias de erradicación como apoyo a las penicilinas o las tetraciclinas. Helicobacter pylori tiene predilección por metabolizarlo, sus productos de degradación rompen la estructura helicoidal de la bacteria. Tiene el inconveniente de que suministrado de forma aislada no es efectivo.
Para los tratamientos de segunda y tercera línea, se suelen optimizar las dosis de antiácidos y amoxicilina o sustituir ésta por doxiciclina. Algunos tratamientos más empíricos que han reflejado un éxito en la terapia aportan sales de bismuto, levofloxacina o rifabutina. Se indican a continuación algunos de los medicamentos:
- Doxiciclina: Las tetraciclinas generalmente son bacteriostáticas en dosis moderadas, es decir, no matan a la bacteria si no que limitan su crecimiento. Actúan sobre la síntesis de ácidos nucleicos en la sub-unidad ribosómica 30S, siempre y cuando hayan penetrado la pared bacteriana. Tiene la ventaja de ofrecer actividad anti-inflamatoria lo que previene parcialmente la aparición de un tumor si la infección se torna rebelde.
- Rifabutina: Su uso para tratar la helicobacter no es muy extendido y se emplea en tratamientos de 4º línea. Es muy exclusiva debido a sus efectos secundarios, ya que un 22% de los pacientes que la toman presentan mielotoxicidad, es decir, se quedan anémicos. Es muy efectiva, se une a la subunidad ribosómica beta y entorpece la síntesis de ARN.
- Levofloxacino: La bacteria Helicobacter es bastante resistente a ello, de ahí que se usen grandes dosis y siempre acompañado de otro antibiótico. Impide la síntesis de ADN. Tengo que aclarar que es un medicamento peligroso, presenta efectos secundarios indeseables como mialgias, fragilidad musculotendinosa y neuropatías. Es bueno que el médico nos lo comente en caso de utilizarlo. Aquí tenéis una revisión sobre ello.
- Sales de bismuto: El principio activo es subsalicilato de bismuto. Tiene propiedades antibacterianas. Se emplea para regular el pH y prevenir las diarreas provocadas por los antibióticos.
- Ranitidina. Es un fármaco inhibidor de los receptores H2 de histamina de las células parietales. Tiene una semivida más larga que el omeprazol, sin embargo no es tan efectiva para neutralizar el ácido y prevenir la ulceración como éste. Su ventaja es que no perjudica la absorción de minerales y vitaminas del grupo B.
Tratamientos naturales para Helicobacter Pylori
La experiencia médica y naturista ofrece también muy buenos resultados, aunque debemos contemplarlo como refuerzo al tratamiento farmacológico o como medida preventiva.
Algunos alimentos y complementos alimenticios mejoran la actividad de los fármacos y debilitan la actividad de la bacteria. Como digo, son efectivos usados como refuerzo. Dejo destacados abajo los siguientes:
- Probióticos: No hay un consenso sólido sobre si los probióticos son claves en la erradicación de la Helicobacter, sin embargo, se sugiere su utilización. En primer lugar van ayudarnos a reconstruir la flora del colon, ejercen competencia a otras bacterias y combaten las infecciones por hongos. El uso de penicilinas deja el camino abierto para que cándidas oportunistas se asienten en el intestino grueso y supongan un dolor de cabeza meses después de tomarlas. Recordad que la penicilina se extrae de un hongo, como casi todos los antibióticos.
- Sulforafano. Los isoticianatos del brócoli, la escarola, las endivias o la rúcula ejercen una actividad antimicrobiana muy interesante. Aclaro que deben tomarse crudas estas verduras, o ligeramente hervidas, ya que sus principios activos se esfumarían.
- Clorofila. Los vegetales de hoja verde como los anteriores, a los que se suma la lechuga batavia, las espinacas, acelgas, repollo y col rizada. Favorecen la regeneración de la mucosa en caso de úlceras y ayudan a regular el pH. Son coadyuvantes de la terapia medicamentosa, pues los antibióticos necesitan pH alto para que tengan más poder.
- Vitamina D y selenio. Aconsejo suministrar estos nutrientes por medio de un suplemento. Nos van a ayudar a que el sistema inmunitario esté más fuerte y protegido. Tanto para combatir la infección como para prevenir la integridad del intestino, pues con los antibióticos quedará expuesto a muchos gérmenes.
- Glutamina. Se ha hablado ya de su poder cicatrizante. Además de colaborar en tareas de limpieza, como deshacerse de los depósitos de amoníaco, ayuda a regenerar la mucosa del estómago. El 90% de la glutamina ingerida se la quedan los enterocitos, así que habrá que suplementarse con 1000 mg diarios mínimo, durante todo el tratamiento. Posteriormente también, al menos 15 días.
- Especias. Orégano, romero, perejil y clavo. Deben aportarse como extracto seco, no en las comidas, ya que la cantidad de principio activo que tomamos es ridícula. Son antimicrobianas y nos serán de utilidad para desparasitar el estómago. De lo mejor que existe en materia de prevención. El clavo es una especia que estimula la liberación de HCL, por ello hay que tomarlo en cápsulas con envoltura vegetal para que pasen inalteradas por el estómago.
- Té de limón. Siempre que no haya úlcera. En caso de gastritis o úlceras activas no deben tomarse frutas ácidas, a pesar de lo que recomiendan muchas personas. El limón es ácido y su metabolismo es alcalino, es cierto, sin embargo, aunque se diga que neutraliza los ácidos estomacales, si hay una herida abierta puede generar una sintomatología molesta. Por ello, la persona que quiera utilizar el limón, debe hacerlo mediante té, diluido bien en agua y comprobar si tiene molestias.
- Calcio y magnesio. Minerales fundamentales que colaboran en la elevación del pH en el estómago. Además los antiácidos disminuyen su absorción por lo que hay aumentar su consumo.
- Vitamina B. Los antibióticos y los antiácidos van a entorpecer su asimilación. Especialmente folatos, B12 y piridoxina. Si normalmente es un complemento casi obligatorio para personas sanas, imaginad su relevancia en este tipo de patologías.
Espero que os sea de ayuda esta guía sobre la Helicobacter Pylori, ya sabéis que estoy a vuestra disposición en comentarios. ¡A seguid sanos/as, no lo olvidéis!