La glutamina es un aminoácido con propiedades únicas que se sintetiza en cantidades suficientes para satisfacer las necesidades corporales cuando las circunstancias fisiológicas son normales. Por ello, se ha considerado clásicamente como un aminoácido no esencial. Sin embargo, en los últimos años se ha argumentado convincentemente que la glutamina debe incluirse entre los aminoácidos condicionalmente esenciales, porque bajo condiciones de estrés metabólico como la sepsis, el estrés quirúrgico o el politraumatismo, su demanda aumenta y el ser humano es incapaz de sintetizarla en cantidades adecuadas.
La glutamina es el aminoácido más abundante en la sangre y en las células. Constituye el 61% de los aminoácidos del músculo esquelético, por lo que representa la mitad del total de los aminoácidos corporales. La glutamina, junto con la alanina, transportan más de la mitad del nitrógeno de los aminoácidos circulantes.
La utilización clínica de la glutamina está indicada en situaciones catabólicas graves. En estos casos, administrada en soluciones parenterales como dipéptido, puede ser de gran utilidad en tejidos con gran intensidad de proliferación (mucosa intestinal, linfocitos, etcétera) y su aporte exógeno puede frenar la salida de este aminoácido desde sus reservas musculares. De esta forma se evita la depleción muscular en glutamina, la atrofia de las vellosidades intestinales y la necrosis intestinal.
Principal objetivo de la glutamina: el intestino
El intestino utiliza el 25% del flujo sistémico de glutamina. En este órgano, la glutamina es el principal sustrato energético y la molécula precursora de ornitina, citrulina, prolina y arginina, así como de nucleótidos y de otras moléculas implicadas en la glicosilación de proteínas.
La glutamina parece desempeñar un papel regulador del crecimiento y diferenciación de la mucosa intestinal a través de la activación de proteín quinasas implicadas en el ciclo celular.
Varios estudios en humanos utilizando NP con soluciones que contienen glutamina han demostrado que la administración de este aminoácido eleva los niveles plasmáticos de glutamina y mejora el balance nitrogenado, aunque no en todos los casos se ha podido constatar un beneficio clínico. Por el contrario, la administración de suplementos de glutamina por vía enteral no mejora ni la mortalidad ni la morbilidad de recién nacidos pretérmino.
Un efecto posible de la glutamina es su influencia en la síntesis de aminoazúcares y, como consecuencia, en la síntesis de proteínas de la matriz extracelular y en la estructura de la mucosa, especialmente de las uniones cerradas (tight junctions). Además, como molécula precursora de aminoazúcares, la glutamina puede desempeñar un papel fundamental en la síntesis de mucina y, por tanto, en el mantenimiento de la integridad de la mucosa.
Glutamina y procesos catabólicos
En varios estados catabólicos como el trauma grave, la sepsis, el trasplante de médula ósea, la quimioterapia intensiva y la radiación, los niveles plasmáticos de glutamina disminuyen. Las alteraciones que se producen en el flujo de glutamina entre órganos durante los estados catabólicos se esquematizan en la siguiente figura.
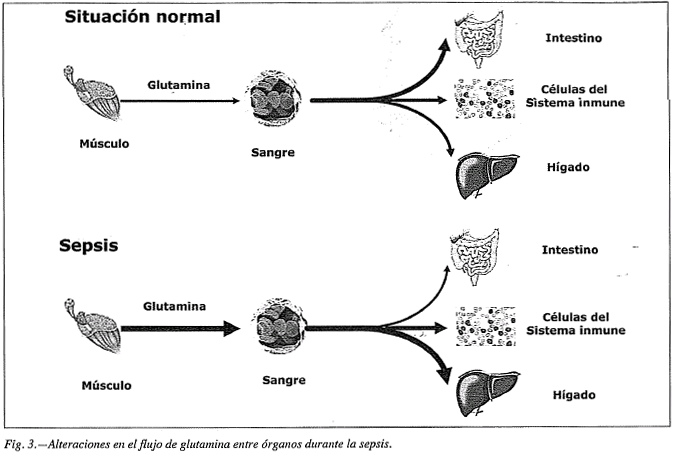
En estas situaciones, se ha demostrado que la administración de glutamina por vía parenteral en forma estable, como dipéptidos solubles alanil-glutamina o glicilglutamina, conjuntamente con otros agentes anabólicos que promueven la captación de nutrientes, es beneficiosa para los pacientes. La administración de glutamina mejora la respuesta al estrés metabólico y el balance nitrogenado. Además, en los pacientes críticos con alteración de la barrera intestinal, la glutamina exógena puede proteger al huésped de las complicaciones derivadas de la endotoxemia. Un posible mecanismo para estos efectos saludables de la glutamina es que contribuya a la síntesis de arginina y, como consecuencia, de óxido nítrico, aumentando la vasodilatación. Otra posibilidad es que estos efectos estén relacionados con la disminución en la expresión de citoquinas proinflamatorias (IL-8 y IL-6) y el aumento en la expresión de citoquinas antiinflamatorias (IL-10) en biopsias intestinales de pacientes que recibieron glutamina por vía enteral.
La administración de dipéptidos permite la esterilización por calor de las soluciones de aminoácidos y el aumento del contenido en glutamina. Por otra parte, los dipéptidos son rápidamente hidrolizados por las hidrolasas presentes en las membranas celulares por lo que son rápidamente aclarados del plasma, sin que existan pérdidas apreciables por orina.
Por lo que se refiere a la glutamina administrada de forma enteral, se ha descrito que consigue disminuir los costes y la duración de las estancias hospitalarias de pacientes críticos. Además, mejora la función inmunológica (por disminución de la respuesta inflamatoria) y la morbilidad de pacientes con trauma múltiple.
Varios estudios clínicos han demostrado que la administración de glutamina restaura la función de las células NK y mejora el metabolismo proteico en los pacientes. Además, la glutamina aumenta la selectividad de los fármacos antitumorales al proteger al paciente del daño oxidativo a través de un aumento del glutatión celular. Por otro lado, en estudios con pacientes con cáncer que reciben radioterapia no se han observado efectos saludables derivados de la administración de glutamina, por lo que actualmente no existe consenso sobre el uso de glutamina en estos pacientes. No obstante, en un análisis reciente de las evidencias clínicas para el uso de nutrición enteral con glutamina se ha observado que es útil en la mejora de la mucositis en pacientes que han recibido quimioterapia.
Bibliografía:
http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0212-16112006000500003

